Что такое интерфероны, как они действуют и когда их примененяют?
Справиться с вирусными инфекциями бывает очень сложно. Но в самом нашем организме есть «встроенная» система противовирусной защиты. Это специальные вещества, интерфероны. Чтобы помочь организму справиться с болезнью, медицина создала лекарственные препараты — искусственные интерфероны и стимуляторы их синтеза, о которых пойдет речь в этой статье.
Содержание статьи:
Функции и механизм действия интерферона в человеческом организме
Интерферон — это белковая молекула, которая обеспечивает противовирусный иммунитет. При этом она обладает неспецифической активностью, то есть действуют не на возбудителя какого-то конкретного заболевания, а на все вирусные частицы в целом. Если сказать обобщенно, то интерферон — универсальный защитник организма, который начинает действовать еще до того, как в работу включатся остальные звенья иммунитета[1]. Препараты интерферона применяются даже в терапии онкологии: они подавляют опухолевый рост.
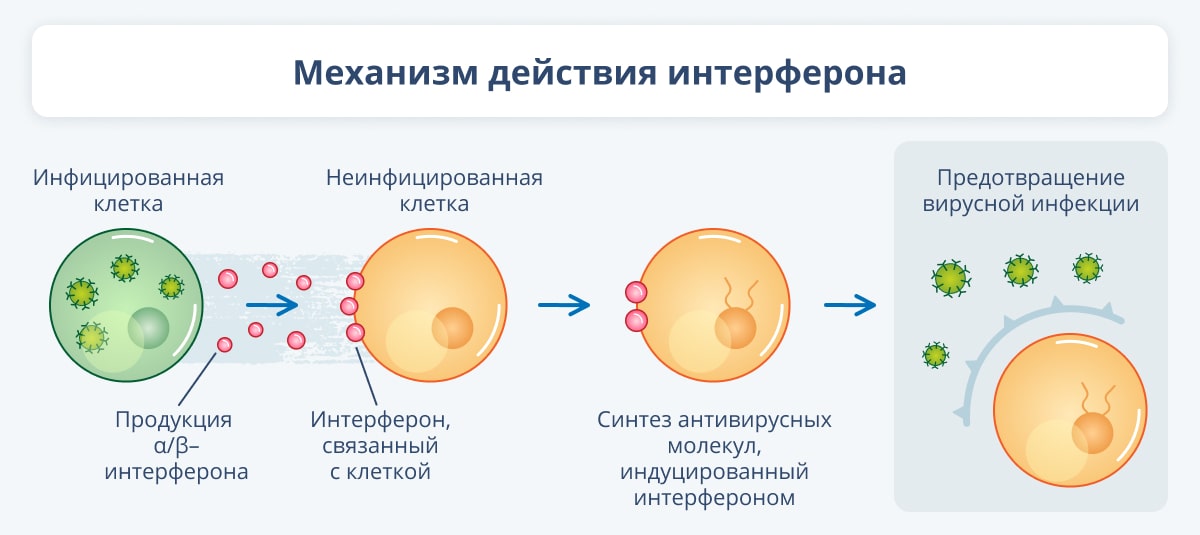
Клетки вырабатывают этот защитный белок в ответ на действие вирусов, бактерий, опухолевых клеток или продуктов их метаболизма. Стимулировать их выработку могут и лекарственные препараты — индукторы интерферона. Молекулы последних, попадая в кровь и межклеточную жидкость, связываются с рецепторами зараженных или поврежденных клеток. Они запускают сложный каскад реакций, приводящих к образованию специфических белков. В результате клетка перестает воспроизводить вирусные частицы, расщепляет их генетическую структуру, а поверхность этой клетки становится менее проницаемой для внутриклеточных паразитов.
Кроме действия на сами зараженные клетки, интерфероны стимулируют активность других звеньев иммунитета, контролируют воспалительную реакцию[2] и даже могут защитить организм от опухолей. Это свойство активно изучают и уже используют для борьбы с некоторыми видами рака[3].
Виды человеческого интерферона
Молекулы интерферона отличаются между собой по генетической структуре, типу клеточных рецепторов, на которые они действуют, даже по участкам ДНК, которые кодируют их состав. Все интерфероны делят на 3 типа.
- К первому типу относят альфа-интерферон, который имеет 13 различных структурных вариантов, а также бета-, каппа-, эпсилон- и омега-.
- Второй тип представлен только одним типом, гамма-интерфероном.
- Относительно недавно, в 2002 году, был открыт и третий тип молекул, лямбда-. Это отдельное семейство интерферонов, которое отличается от всех предыдущих генетическим строением и даже типом рецепторов, с которыми они взаимодействуют. Но по своей биологической активности лямбда-интерфероны очень похожи на первый тип[4].
Не стоит относиться к интерферонам как к панацее от всех бед. Во-первых, некоторые вирусы могут подавлять образование специфических белков внутри зараженных клеток, что значительно снижает эффективность противовирусной защиты.
Во-вторых, это лишь первая «линия обороны», которая стимулирует другие звенья иммунитета и временно приостанавливает продвижение «врага» по организму, давая время на выработку иммунных клеток и антител.
В-третьих, основной механизм действия интерферона — это подавление развития и деления. В физиологических дозах этот эффект контролирует размножение вирусов и опухолевых клеток. Но при введении значительных доз «чужеродного» вещества могут пострадать и собственные ткани организма, которые быстро обновляются. В первую очередь — клетки крови.
Поэтому прежде чем начинать лечение препаратами интерферона, нужно внимательно изучить пользу и возможный вред от их приема.
Применение аналогов интерферона в медицине
Лекарственные средства на основе интерферона доказали свою эффективность[5] в лечении широкого круга заболеваний: герпетических инфекций, ВПЧ, острых и хронических форм вирусного гепатита, рассеянного склероза, волчанки, гриппа и многих других вирусных и бактериальных инфекций. Применяют интерферон и при терапии онкологических заболеваний, а также СПИДа. И это притом, что по меркам медицины открыли его совсем недавно. Это произошло в 1957 году при проведении опытов на мышах. Ученые обратили внимание, что животные, заразившиеся одним вирусом, становились невосприимчивы к другому вирусному заболеванию. Это явление было названо интерференцией, а вещества, которые ему способствовали — интерферонами. Оказалось, что интерфероны вырабатываются не только у мышей, но и у всех млекопитающих, в том числе у человека. Началось изучение возможности промышленного производства веществ, обладающих противовирусным эффектом.
Однако долгое время применение интерферонов было ограничено из-за несовершенства процедуры их получения. Выделять это вещество из крови человека-донора было сложно, дорого и неэффективно.
В 1 литре крови донора содержится всего 1 мкг интерферонов. Примерно такое количество этих молекул нужно для того чтобы изготовить всего одну дозу препарата[6]. А за курс лечения тяжелых вирусных заболеваний, таких как гепатит, человек может получить около 150 доз[7].
В 1980 году в Японии впервые использовали для производства интерферона специально выращенную культуру лимфобластных клеток. А в 1981 году в США вместо клеток человека использовали культуру дрожжевых грибков. С помощью генной инженерии в геном ввели ген, который кодирует производство молекулы интерферона. Это позволило значительно упростить производство препарата[8].
По способу производства существует четыре основных разновидности этого препарата: лейкоцитарный, лимфобластоидный, рекомбинантный и пегилированный.
Лейкоцитарный интерферон получают из крови доноров. Для того чтобы усилить выработку нужных веществ, клетки предварительно стимулируют чаще всего с помощью непатогенных вирусов — таких частиц, которые не могут вызвать заболевание, но при этом воспринимаются клетками иммунной системы как «сигнальные».
После получения такой препарат очищают и концентрируют. В него могут входить все виды интерферонов и другие биологически активные вещества. Это одновременно и плюс, и минус. Преимущество такого препарата — его высокий потенциал биологического действия. Недостаток — высокая вероятность побочных эффектов при внутримышечном введении.
Лимфобластоидный интерферон получают не от человека-донора, а из культуры лимфобластных клеток, которые также обрабатывают веществами, стимулирующими иммунный ответ. Такие препараты содержат определенное соотношение различных видов интерферона и не так часто вызывают побочные эффекты.
Рекомбинантные препараты получают из культуры клеток бактерий или грибов, в которые специально внедрили участок человеческого гена. Интерферон, полученный таким образом, может немного отличаться по своему строению от «природного» человеческого. Такие препараты сохраняют противовирусную активность, но стимуляции иммунитета с их помощью добиться сложно[9].
Пегилированные, или ПЭГ-интерфероны — это рекомбинантные белковые молекулы, соединенные с полиэтиленгликолем. Такое соединение увеличило срок действия интерферона в организме.
Если стандартный рекомбинантный интерферон при лечении вирусного гепатита C нужно вводить три раза в неделю, то пегилированный достаточно использовать один раз за то же время[10].
ПЭГ растворим в воде, не вступает в биологические реакции в организме и не вызывает иммунного ответа. При присоединении ПЭГ молекула интерферона значительно увеличивается в размерах. А это, в свою очередь, увеличивает период полувыведения препарата.
Препараты на основе интерферона: показания и противопоказания к их применению
Объединить интерфероны в однородные группы по методу получения, формам выпуска и показаниям не получится. Каждый препарат имеет свои особенности применения, эффективность при определенных заболеваниях. В зависимости от степени очистки и других факторов какие-то препараты с одним и тем же видом иммуноглобулина могут применяться только местно, а какие-то можно использовать в виде инъекций.
Например, такие препараты как «Инферон» и «Альфаферон» относят к группе лейкоцитарных интерферонов. При этом «Инферон»[11] согласно инструкции применяют внутримышечно при неуточненных вирусных заболеваниях и для иммунотерапии. «Альфаферон»[12] тоже вводят в мышцу, но при этом уже используют для лечения гепатита, микоза и даже некоторых онкологических заболеваний. А «Интерферон человеческий лейкоцитарный»[13] используют для местного применения, закапывания в нос и проведения ингаляций.
Поэтому при выборе препарата интерферона стоит ориентироваться не только на общую характеристику группы веществ, но в первую очередь на рекомендации врача и инструкцию по применению конкретного препарата.
Интерферон в виде инъекций применяют при системных заболеваниях, таких как гепатит, опухоли или рассеянный склероз. Препарат в виде капель в нос подходит для лечения риносинуситов и профилактики ОРВИ. Капли в глаза помогут при конъюнктивите. Суппозитории можно использовать при многих заболеваниях, в том числе у детей. А гель подходит для смазывания носа или кожи.
Одной из наиболее однородных групп на сегодняшний момент являются пегилированные интерфероны. Существует два основных класса препаратов с доказанной эффективностью[14] — это пегинтерферон альфа-2а и пегинтерферон альфа-2b. Представитель первого класса — «Пегасис»[15], второго — «ПегИнтрон»[16]. Оба препарата используют подкожно, один раз в неделю и применяют только для лечения хронического вирусного гепатита В и С.
Рекомбинантный интерферон — одна из самых многочисленных по торговым наименованиям групп препаратов.[17] Сюда относятся такие лекарства как «Реаферон», «Виферон», «Ингарон», «Интерфераль» и другие. Эти препараты имеют различные формы для местного применения и для инъекций. У каждого препарата в инструкции определен свой перечень показаний, но в целом — это вирусные и бактериальные инфекции.
Интерфероны защищают организм от вирусов, бактерий и опухолевых клеток. Они обладают сложным биологическим действием. Но современная медицина научилась создавать аналогичные вещества и использовать их. Однако подбор подходящего препарата — задача, которую может решить только врач.